
目前国内流感疫苗渗透率低,与发达国家仍有巨大差距,国内流感疫苗仍存在巨大的成长空间。美莱德拥有完善的流感疫苗一站式生物分析服务,可对临床试验生物样本进行全流程监管,降低项目管理难度,提高研发效率,加速流感疫苗产品的上市进程,为流感疫苗的研发提供有力支持。

小编将会从以上流感疫苗生物分析的五大板块为大家分期介绍,往期回顾:

1、MDCK(NBL-2)细胞库建立
MDCK(Madin Darby Canine Kidney)细胞是流感病毒进行复制的细胞系之一,该细胞系用于对流感病毒分离培养的敏感性高于VERO等其它细胞系,MDCK细胞的培养是进行流感病毒分离和培养的基本实验技术。我司生物分析中心从中国典型培养物保藏中心(CCTCC)购得原始细胞株,用于病毒的扩增及检测,并按2020版药典中《生物制品生产检定用动物细胞基质制备及质量控制》要求进行了初级细胞库和主细胞库的建立,已完全满足后续扩毒及检测用细胞的用量。
 流感病毒对鸡胚和MDCK细胞均较敏感,目前市场上流感疫苗主要为鸡胚培养疫苗、细胞培养疫苗和小部分重组疫苗。我司生物分析中心从2022年开始,每年从NIBSC购入当年WHO宣布的流感病毒疫苗的推荐株(包含A型H1N1株、A型H3N2株、B型Victoria系、B型Yamagata系)以及毒株配套抗原和抗血清。根据具体毒株推荐扩增方式,按照中国疾病预防控制中心在2007年发布的《国家流感中心标准操作规程》和WHO在2011年发布的《流感实验室诊断和病原学监测手册》中细胞和鸡胚培养的病毒分离标准操作规程进行了病毒扩增和传代,已完成全部毒株的初级病毒库、主病毒库、工作病毒库的建立,能完全满足实验需求,见下表1。
流感病毒对鸡胚和MDCK细胞均较敏感,目前市场上流感疫苗主要为鸡胚培养疫苗、细胞培养疫苗和小部分重组疫苗。我司生物分析中心从2022年开始,每年从NIBSC购入当年WHO宣布的流感病毒疫苗的推荐株(包含A型H1N1株、A型H3N2株、B型Victoria系、B型Yamagata系)以及毒株配套抗原和抗血清。根据具体毒株推荐扩增方式,按照中国疾病预防控制中心在2007年发布的《国家流感中心标准操作规程》和WHO在2011年发布的《流感实验室诊断和病原学监测手册》中细胞和鸡胚培养的病毒分离标准操作规程进行了病毒扩增和传代,已完成全部毒株的初级病毒库、主病毒库、工作病毒库的建立,能完全满足实验需求,见下表1。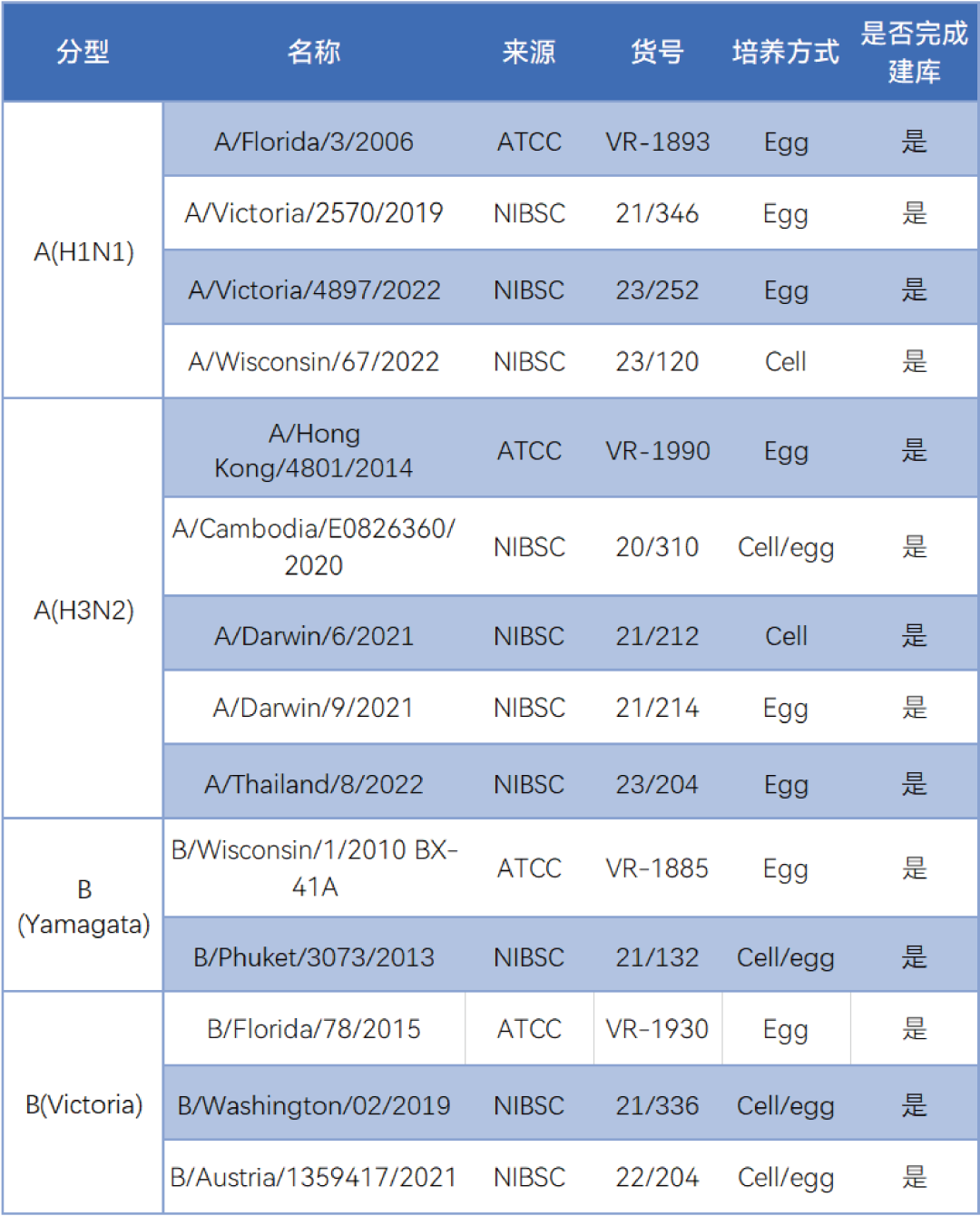
表1 美莱德储备的流感病毒株
鸡胚分离流感病毒简要步骤为:取9-11日龄SPF鸡胚,选择适宜病毒浓度注射接种至鸡胚尿囊腔,蜡封注射口,将鸡胚置于35℃温箱培养2~3天,病毒培养完成后在无菌环境吸取鸡胚尿囊液。该方法收获病毒液产量大;滴度高,滴度能达107TCID50/mL以上;稳定性好,-80℃冰箱冻存2年内长期稳定。MDCK细胞分离流感病毒简要步骤为:通用按照《国家流感中心标准操作规程》和《流感实验室诊断和病原学监测手册》方法,接种适宜病毒至提前培养好的MDCK细胞中,置于二氧化碳培养箱培养2~3天,病毒培养完成后离心收获。我司分析中心对病毒培养液成分、培养温度、培养时间等进行条件优化,大大提高病毒扩增效率和滴度。单批可收获病毒量最多为1000mL、病毒滴度水平维持107TCID50/mL以上且长期冻存稳定性较好。我司生物分析中心已完成流感疫苗推荐毒株的初级病毒库、主病毒库、工作病毒库的建立,并先后开发和验证了血凝法(HA)、蚀斑法、细胞半数感染量法(TCID50)、间接免疫荧光定量测定法(FFA)等系列检测流感病毒滴度的方法,可全方面确定扩增病毒滴度和不同种属生物样本流感病毒滴度检测需求,具备丰富的检测经验,已顺利完成多个雪貂的流感疫苗减毒特性研究项目和疫苗免疫原性及攻毒保护力试验项目等。美莱德不仅拥有专业的生物分析团队,还拥有药学研究服务,可为流感疫苗的研究提供全方位咨询和实验技术服务。下期我们将为大家分享:MED药学研究 | 美莱德流感疫苗研发一站式服务(六)—— 下一代候选流感疫苗及潜力,敬请期待![1] 中国流感疫苗预防接种技术指南(2023-2024)。[2] Manual for laboratory diagnosis and virological surveillance of influenza,WHO, 2011.[5] 流行性感冒诊断标准,WS 285-2008。


















