

流行性感冒是一种由流感病毒引起的丙类传染病。其主要由甲型和乙型流感病毒导致,其中在中国甲型流感最常见。感染流感病毒后,病毒通过与呼吸道表面细胞结合进入细胞并复制,导致全身症状如发热、头痛、肌痛等。流感病毒的抗原变异特性使得它的传染性强,人群普遍易感,且同一人群可以多次感染。流感病毒适应冷、湿气候,其在冬春季多见。

目前国内流感疫苗渗透率低,与发达国家仍有巨大差距。截至 2020 年,国内流感疫苗批签发总量达到了 5765 万剂次,若按照 2020 年末全国总人口 141212 万人来计算,即便当年签发的疫苗实现全部接种,全人群接种率也仅有 4.08%。以美国为例,在2022-23流感季节,6个月至17岁儿童中≥1剂流感疫苗的接种覆盖率为57.4%,18≥岁的成年人流感疫苗接种覆盖率为 46.9%,65 岁以上的老年人流感疫苗接种覆盖率则达到 73.9%。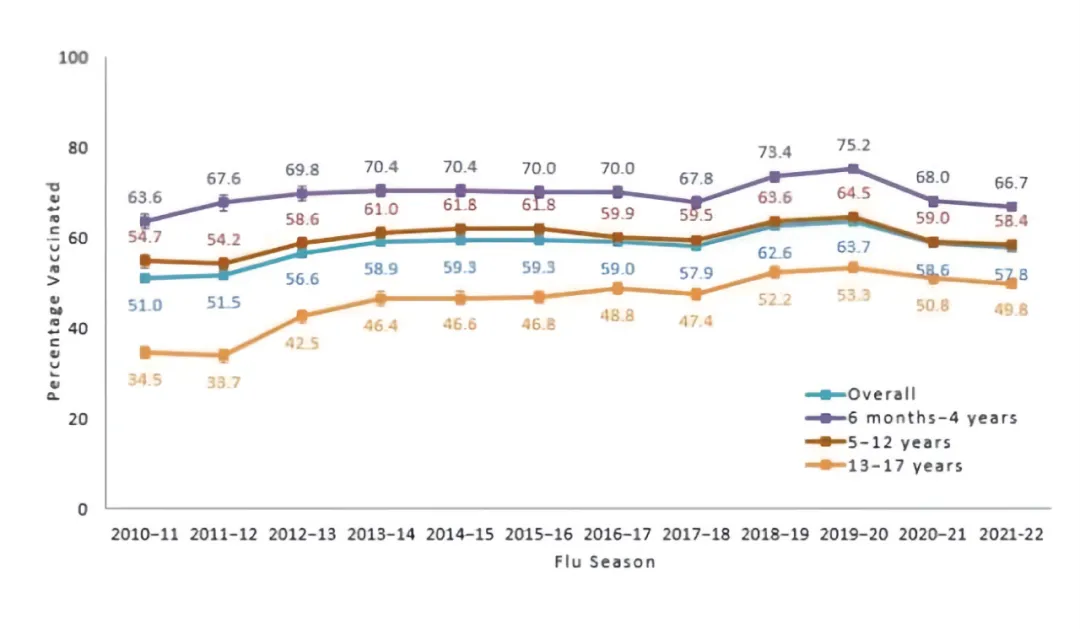
若参考美国的成年人全人群接种率,按 50%来测算国内市场的天花板,则按中国 2022 年末总人口 141175 万人测算,需要的流感疫苗接种率约为 7 亿剂次, 2020 年之前的批签发量不足 1/10,国内流感疫苗仍存在着巨大的成长空间。
 小编将会从以上流感疫苗一站式生物分析的五大板块为大家分期介绍,本期为大家分享血清HI抗体水平检测。
小编将会从以上流感疫苗一站式生物分析的五大板块为大家分期介绍,本期为大家分享血清HI抗体水平检测。 红细胞凝集抑制试验简称血凝抑制试验,血凝抑制试验最初在 1942 年由 Hirst 提出,1944 年被 Salk 改进,现在是世界卫生组织(WHO)推荐使用的微量测定法。当病毒悬液中加入特异性抗体,且这种抗体的量足以抑制病毒颗粒或其血凝素时,红细胞表面的受体就不能与病毒颗粒或血凝素直接接触。这时红细胞的凝集现象就被抑制,成为红细胞凝集抑制(HI)反应,也称血凝抑制反应。血凝抑制试验的基本原理是流感病毒能引起红细胞凝集主要是由于流感病毒表面的血凝素与红细胞表面的受体结合,病毒被吸附到红细胞上而产生的。但这一过程可被某些物质所抑制。如血清中血凝素抗体能够与病毒血凝素分子的抗原位点特异性结合,干扰病毒血凝素与红细胞上受体的结合过程,从而抑制红细胞凝集。
红细胞凝集抑制试验简称血凝抑制试验,血凝抑制试验最初在 1942 年由 Hirst 提出,1944 年被 Salk 改进,现在是世界卫生组织(WHO)推荐使用的微量测定法。当病毒悬液中加入特异性抗体,且这种抗体的量足以抑制病毒颗粒或其血凝素时,红细胞表面的受体就不能与病毒颗粒或血凝素直接接触。这时红细胞的凝集现象就被抑制,成为红细胞凝集抑制(HI)反应,也称血凝抑制反应。血凝抑制试验的基本原理是流感病毒能引起红细胞凝集主要是由于流感病毒表面的血凝素与红细胞表面的受体结合,病毒被吸附到红细胞上而产生的。但这一过程可被某些物质所抑制。如血清中血凝素抗体能够与病毒血凝素分子的抗原位点特异性结合,干扰病毒血凝素与红细胞上受体的结合过程,从而抑制红细胞凝集。 具体实验操作流程:试验准备-测定抗原HA效价-四单位抗原的配制及验证-倍比稀释待检血清-加入四单位抗原-抗原抗体作用-加入红细胞反应-读取结果。取待测血清加入RDE(Ⅱ)37℃水浴过夜后,再加入PBS。HA即血凝试验,是进行HI试验必须具备的步骤。首先要测定所使用抗原的血凝价,便于后续配置四单位抗原。测定好抗原的血凝价后,就可制备四单位抗原了。完成制备后,要对四单位抗原进行验证,确保制备的精确性。(4个凝集单位/25微升)。在96孔血凝板内加入PBS,再加入待测血清进行2倍倍比稀释。在稀释好的板内,每孔加入25微升经验证的四单位抗原液。抗体抗原作用完毕后,就可以加1%红细胞了,每孔50微升,注意加的时候吸头尽量垂直于血凝板,在其上方0.5cm处,以免造成污染。
具体实验操作流程:试验准备-测定抗原HA效价-四单位抗原的配制及验证-倍比稀释待检血清-加入四单位抗原-抗原抗体作用-加入红细胞反应-读取结果。取待测血清加入RDE(Ⅱ)37℃水浴过夜后,再加入PBS。HA即血凝试验,是进行HI试验必须具备的步骤。首先要测定所使用抗原的血凝价,便于后续配置四单位抗原。测定好抗原的血凝价后,就可制备四单位抗原了。完成制备后,要对四单位抗原进行验证,确保制备的精确性。(4个凝集单位/25微升)。在96孔血凝板内加入PBS,再加入待测血清进行2倍倍比稀释。在稀释好的板内,每孔加入25微升经验证的四单位抗原液。抗体抗原作用完毕后,就可以加1%红细胞了,每孔50微升,注意加的时候吸头尽量垂直于血凝板,在其上方0.5cm处,以免造成污染。
图2(抗体效价为5120及320)

2、流感病毒HI方法学验证
面对已建立的方法学,我司生物分析中心主要从LOD值、准确度、精密度三个验证指标进行了考察,目前已完成雪貂及大鼠的HI方法学验证并完成验证报告的撰写。选择不少于20份阴性 雪貂/大鼠血清样本进行考察。进行连续3批检测,采用3个批次检测结果算得LOD值。
通过稀释阳性雪貂/大鼠血清样本后在不同的稀释倍数对应不同浓度水平得到的HAI抗体滴度值来确定试验方法的准确性。通过稀释阳性雪貂/大鼠血清样本后在高滴度及低滴度两个不同浓度水平的样本由不同人员及不同天测得的HAI抗体滴度值来确定试验方法的重复性及重现性。
重庆美莱德生物分析中心建立了红细胞凝集抑制法(HI)检测血清中HI抗体滴度的方法,来检测雪貂、大鼠、小鼠、人血清中HI抗体滴度。依据CDE《疫苗临床试验抗体分析方法研究技术指导原则(征求意见稿)》等相关法规进行了方法学验证(Cut-off(临界值)/LOD值、准确度、精密度)等指标进行了全面的验证,完成了符合申报要求的验证报告。本期为大家分享了:美莱德流感疫苗研发一站式服务(一)—— HI法检测血清样本中HI抗体的检测流程及方法学验证下期将为大家分享:美莱德流感疫苗研发一站式服务(二)—— 流感中和抗体检测方法学分享,敬请期待![1] 格罗什科普夫拉,布兰顿LH,费迪南德JM,钟JR,布罗德KR,塔尔博特香港。用疫苗预防和控制季节性流感:美国免疫实践咨询委员会的建议,2023-24流感季节。MMWR建议代表2023;72:1-25.[2] 疾病控制中心。不同季节流感疫苗接种覆盖率。2023.



















